点评丨朱冰(中国科学院生物物理研究所)、高绍荣(同济大学)
异染色质在转录抑制和基因组稳定性维持中发挥重要作用【1-4】。细胞增殖过程中异染色质结构保持稳定,该稳态依赖H3K9me3表观遗传【5-8】。DNA复制后,由于插入了新合成的非修饰组蛋白,导致H3K9me3丰度被稀释至约初始一半水平【9-11】。H3K9me3阅读器HP1是异染色质结构蛋白,包含Chromo domain(CD)和Chromo shadow domain(CSD)两个结构域,CD可识别已有的H3K9me3,CSD可发生二聚化并招募H3K9me3的甲基转移酶SUV39H1,被招募的SUV39H1进而催化邻近核小体发生H3K9me3修饰,形成HP1-SUV39H1介导的“读-写”正反馈循环【12-15】。此外,SUV39H1自身也含有CD结构域,可直接识别已有H3K9me3并进一步修饰邻近核小体【16-18】。以上两个层面的“读-写”正反馈机制协同促进DNA复制后的H3K9me3在细胞周期中的重建。
H3K9me3过度修饰易导致细胞发生有害的过度异染色质化,因此H3K9me3重建过程中的“读-写”正反馈需受到严格限制。裂殖酵母中Clr4(人类SUV39H1/2的同源基因)已被报道具有自抑制构象,可防止其甲基转移酶过度活化【19】,但在哺乳动物体细胞中,限制H3K9me3表观遗传以保障异染色质稳态的具体机制仍鲜为人知。
2025年5月30日,中山大学肿瘤防治中心康铁邦/武远众团队在Science发表了题为ASB7 is a negative regulator of H3K9me3 homeostasis的研究论文。该工作揭示了E3泛素连接酶CUL5ASB7发挥刹车器角色,通过细胞周期依赖性降解SUV39H1来保障H3K9me3在细胞周期中精准重建,进而维持异染色质在细胞增殖过程中的结构稳定。

KDM4家族是H3K9me3的去甲基化酶,可在受精卵的合子基因组激活前阶段对H3K9me3进行大规模擦除,这一过程是表观遗传重编程的关键步骤,为胚胎基因组的激活提供开放的染色质环境。但在体细胞中,作者将KDM4A/B/C同时敲除,经过多个有丝分裂周期,观察到H3K9me3水平仍然保持恒定,提示体细胞中KDM4介导的去甲基化基本不参与限制H3K9me3表观遗传。为系统性揭示H3K9me3的调节因子,作者利用全基因组CRISPR-Cas9文库进行遗传学筛选,发现E3泛素连接酶CUL5ASB7是限制H3K9me3表观遗传的关键因子。
机制上,HP1通过其CSD结构域募集ASB7至异染色质,异染色质定位的ASB7可促进SUV39H1泛素化降解,并且该降解过程受到严密的细胞周期控制。在S期及G2期,ASB7处于非磷酸化状态,可有效结合并降解SUV39H1,从而限制H3K9me3过度修饰及延伸;进入有丝分裂M期后,CDK1-Cyclin B1迅速激活并磷酸化ASB7的底物识别结构域,进而阻断ASB7与SUV39H1互作,使得SUV39H1蛋白水平在M期达到顶峰,促进了H3K9me3在M期及G1期的重建,这一机制保障了H3K9me3在下一个S期开始之前精准恢复至初始水平。
总的来说,该研究发现在哺乳动物体细胞DNA复制后的H3K9me3表观遗传过程中,ASB7发挥刹车器角色,通过HP1-SUV39H1-ASB7介导的“读-写-降解”平衡,而非经典HP1-SUV39H1-KDM4介导的“读-写-擦除”平衡,控制着H3K9me3进行细胞周期依赖性精准重建。
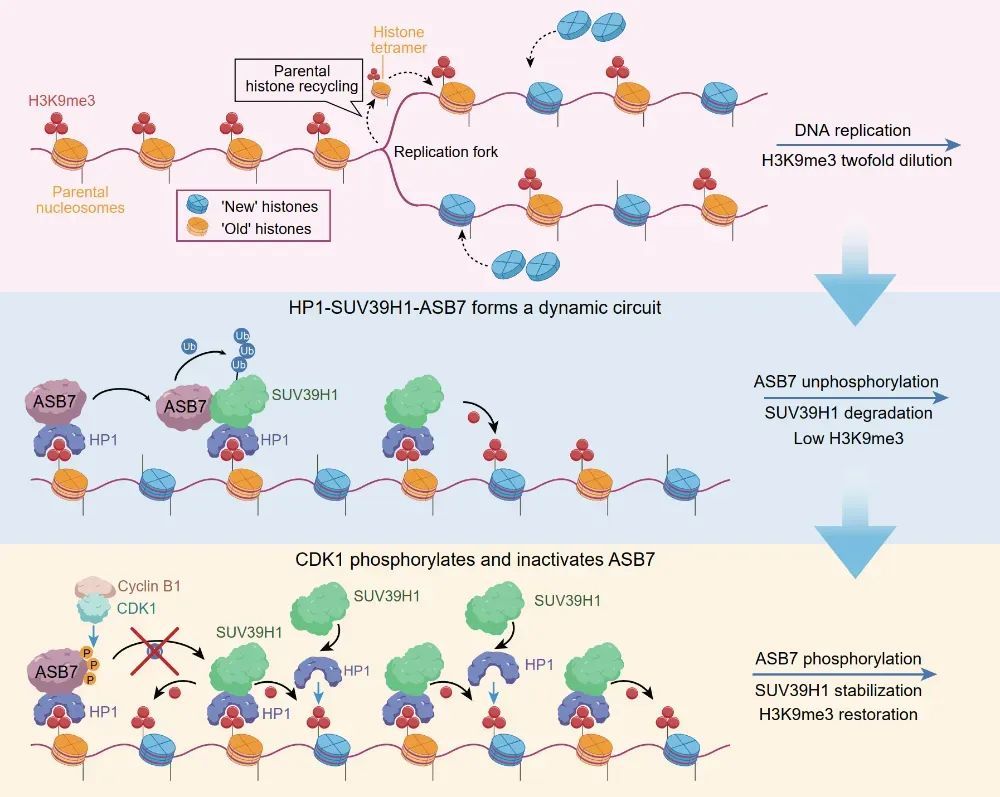
模式图:HP1-SUV39H1-ASB7介导的“读-写-降解”平衡控制H3K9me3表观遗传
H3K9me3及异染色质稳态失调会导致基因组不稳定。作者发现ASB7在多种肿瘤中呈现扩增状态,ASB7高表达引起H3K9me3水平降低,进而导致同源重组修复受损及基因组不稳定。这一现象提示,ASB7扩增型肿瘤患者可能是PARP抑制剂的潜在获益人群。
中山大学肿瘤防治中心周立文副研究员、陈振轩硕士研究生、中山大学医学院邹叶子博士研究生为该论文共同第一作者。中山大学肿瘤防治中心康铁邦研究员、武远众副研究员为该论文通讯作者。中国科学院生物物理研究所朱冰研究员、北京大学尹玉新教授、中国科学院上海药物研究所周虎研究员和朱洪文副研究员、中山大学高嵩研究员等在项目的实施、修稿等过程中,提供了重要的帮助。
专家点评
朱冰(中国科学院生物物理研究所)
H3K9甲基化修饰在表观遗传领域有着特殊重要的地位,不仅仅因为它是重要的异染色质分子标记且抑制转录活性,还因为它与两个重要的里程碑事件密切相关:1. H3K9甲基化在功能上与1930年发现的首个经典表观遗传学现象PEV(Position effect variegation)密切相关,PEV的发现者Hermann Muller于1946年获得诺贝尔奖;2. H3K9甲基化酶是首个被发现的组蛋白甲基化酶,在Thomas Jenuwein实验室2000年的这一发现之前,组蛋白甲基化方面的研究论文大概只有几十篇,而目前恐怕已经有几万到几十万篇(BioArt注:恐怕略有夸张。)。
SUV39家族的H3K9甲基化酶及其相互作用伙伴HP1都有结合H3K9甲基化修饰的能力,因此这一催化体系有着“复制粘贴”的能力,可以实现H3K9甲基化在基因组上的蔓延。那么H3K9甲基化为什么不会蔓延到整个基因组呢?这毫无疑问是细胞必须解决的问题,否则所有的基因都会被沉默,细胞也就无法存活。换言之,异染色质水平的平衡是一个关键的生物学问题(BioArt注:推而广之,是否可以认为染色质领域各种核酸和组蛋白修饰的的水平平衡都是关键科学问题?)。
中山大学康铁邦/武远众研究团队在Science杂志上发表的论文揭示了H3K9甲基化的一种负调控新机制,该机制在异染色质的平衡调控中有着重要作用。他们通过筛选,发现ASB7能够调控H3K9甲基化水平,原因是ASB7可以作为CUL5泛素连接酶复合体的接头蛋白来介导哺乳动物细胞两个SUV39家族蛋白之一的SUV39H1的泛素化和降解,从而实现对H3K9甲基化的负调控。有趣的是,ASB7本身还受细胞周期因子CDK1介导的磷酸化负调控,以确保其在正确的时间发挥作用。
由于ASB7的编码基因经常在肿瘤细胞中发生扩增,该论文进一步发现ASB7编码基因扩增的肿瘤细胞对PARP1抑制剂更为敏感,很可能是这些细胞中发生的H3K9甲基化下调诱发了DNA损伤的同源重组修复缺陷。
该工作与我团队去年发表的由ZNF512介导的异染色质起始机制正好是一个硬币的两面(BioArt注:私货夹带的恰到好处,详见:Nature丨朱冰课题组发现旁着丝粒异染色质的建立机制):异染色质的起始与限制机制。当然,很可能还存在其它机制来调控异染色质的平衡,这也是我们正在探索的方向。
专家点评
高绍荣(同济大学)
H3K9三甲基化(H3K9me3)是异染色质的标志性修饰,与基因沉默、转座子抑制及染色质压缩密切相关。在哺乳动物早期胚胎发育过程中,受精后合子基因组激活(zygotic genome activation, ZGA)是一个关键事件。去甲基化酶KDM4介导的H3K9me3擦除在ZGA前阶段扮演重要角色,为早期发育基因的激活创造了有利的表观遗传环境,维持了基因组的稳定性和适当的表观遗传状态,并参与了母源向合子基因组控制的转换。敲除KDM4会导致H3K9me3清除失败,ZGA关键基因无法激活,引起胚胎发育停滞。
与早期胚胎中KDM4功能截然不同,康铁邦/武远众团队发现在哺乳动物体细胞中敲除KDM4完全不影响H3K9me3表观遗传状态。为揭示体细胞中H3K9me3表观遗传稳态的调控机制,研究人员利用全基因组CRISPR-Cas9文库筛选,发现E3泛素连接酶CUL5ASB7在限制H3K9me3方面发挥关键作用。机制研究表明H3K9me3阅读器HP1可募集ASB7至异染色质,进而泛素化降解SUV39H1,而细胞周期激酶CDK1-Cyclin B1则可磷酸化ASB7并阻断其与SUV39H1结合,从而稳定SUV39H1并介导了H3K9me3在细胞周期中精准重建。
以上机制表明,在哺乳动物胚胎早期发育与体细胞增殖过程中,H3K9me3受到截然不同的调控模式。哺乳动物受精后,父源染色质富含H3K9me3且高度浓缩,需要在ZGA前进行大规模擦除,在此过程中KDM4介导的主动去甲基化发挥关键作用,保障了ZGA前实现开放的染色质环境。而在体细胞中,H3K9me3面临着DNA复制后的被动稀释,需要在随后的细胞周期中重建,此时通过CDK1-ASB7精准控制甲基转移酶SUV39H1的蛋白水平,可以保障H3K9me3在每一个细胞周期中恰好恢复至初始水平。体细胞中的这一机制避免了H3K9me3过度修饰及KDM4介导的擦除过程,该策略可能是哺乳动物进化过程中的一种选择。
总的来说,该研究发现了哺乳动物体细胞中H3K9me3表观遗传新的调控模式,即:通过E3泛素连接酶ASB7介导的降解,而非去甲基化酶KDM4介导的擦除,来控制H3K9me3及异染色质稳态。ASB7异常表达导致了异染色质稳态失调及基因组不稳定,与肿瘤发生发展密切相关。
原文链接:http://doi.org/10.1126/science.adq7408
参考文献:
1.R. C. Allshire, H. D. Madhani, Ten principles of heterochromatin formation and function.Nat Rev Mol Cell Biol19, 229-244 (2018).
2.S. I. S. Grewal, The molecular basis of heterochromatin assembly and epigenetic inheritance.Mol Cell83, 1767-1785 (2023).
3.A. Janssen, S. U. Colmenares, G. H. Karpen, Heterochromatin: Guardian of the Genome.Annu Rev Cell Dev Biol34, 265-288 (2018).
4.J. Padeken, S. P. Methot, S. M. Gasser, Establishment of H3K9-methylated heterochromatin and its functions in tissue differentiation and maintenance.Nat Rev Mol Cell Biol23, 623-640 (2022)
5.J. Nakayama, J. C. Rice, B. D. Strahl, C. D. Allis, S. I. Grewal, Role of histone H3 lysine 9 methylation in epigenetic control of heterochromatin assembly.Science292, 110-113 (2001).
6.J. S. Becker, D. Nicetto, K. S. Zaret, H3K9me3-Dependent Heterochromatin: Barrier to Cell Fate Changes.Trends Genet32, 29-41 (2016).
7.S. Reaet al., Regulation of chromatin structure by site-specific histone H3 methyltransferases.Nature406, 593-599 (2000).
8.D. Moazed, Mechanisms for the inheritance of chromatin states.Cell146, 510-518 (2011).
9.C. Alabertet al., Two distinct modes for propagation of histone PTMs across the cell cycle.Genes Dev29, 585-590 (2015).
10.M. Xu, W. Wang, S. Chen, B. Zhu, A model for mitotic inheritance of histone lysine methylation.EMBO Rep13, 60-67 (2011).
11.A. V. Probst, E. Dunleavy, G. Almouzni, Epigenetic inheritance during the cell cycle.Nat Rev Mol Cell Biol10, 192-206 (2009).
12.M. Lachner, D. O'Carroll, S. Rea, K. Mechtler, T. Jenuwein, Methylation of histone H3 lysine 9 creates a binding site for HP1 proteins.Nature410, 116-120 (2001).
13.A. J. Bannisteret al., Selective recognition of methylated lysine 9 on histone H3 by the HP1 chromo domain.Nature410, 120-124 (2001).
14.C. Maison, G. Almouzni, HP1 and the dynamics of heterochromatin maintenance.Nat Rev Mol Cell Biol5, 296-304 (2004).
15.W. Zeng, A. R. Ball, Jr., K. Yokomori, HP1: heterochromatin binding proteins workingthe genome.Epigenetics5, 287-292 (2010).
16.M. M. Muller, B. Fierz, L. Bittova, G. Liszczak, T. W. Muir, A two-state activation mechanism controls the histone methyltransferase Suv39h1.Nat Chem Biol12, 188-193 (2016).
17.W. Duet al., Mechanisms of chromatin-based epigenetic inheritance.Sci China Life Sci65, 2162-2190 (2022).
18.L. Aagaardet al., Functional mammalian homologues of the Drosophila PEV-modifier Su(var)3-9 encode centromere-associated proteins which complex with the heterochromatin component M31.EMBO J18, 1923-1938 (1999).
19.N. Iglesiaset al., Automethylation-induced conformational switch in Clr4 (Suv39h) maintains epigenetic stability.Nature560, 504-508 (2018).