要说肠道菌群和谁最搭那肯定非代谢组学莫属!肠道菌群可以解答菌群结构变化和疾病/表型关系,而代谢组学可以回答代谢物变化如何介导表型,将他俩结合起来就可以完美解释“菌群结构改变→关键代谢物变化→宿主代谢紊乱→疾病发生”这一因果链。3月18日,广州中医药大学团队在Phytomedicine上发表的文章也用到了这两个组学。

题目:微生物群-色醇-AhR轴介导了护肾痛风泰颗粒对高尿酸血症肾病的肠肾保护作用
这项研究围绕护肾痛风泰颗粒(HSTFT)改善高尿酸血症肾病(HN)的作用机制展开,以肠-肾轴为切入点,通过体内实验先明确了整体效应和菌群/代谢物靶点,再通过体外细胞实验探究通路的细胞层面作用机制,最终打通了“菌群-代谢物-受体”这一调控轴,具体来说就是B.breve(双歧杆菌)→TOL(色氨酸代谢物)→AhR(芳香烃受体)。所以说,选择合适的生信技术,就能帮咱们快速从大量组学数据里挖出核心机制!主要结果
基于UPLC-QTOF/MS鉴定 HSTFT 中化学成分
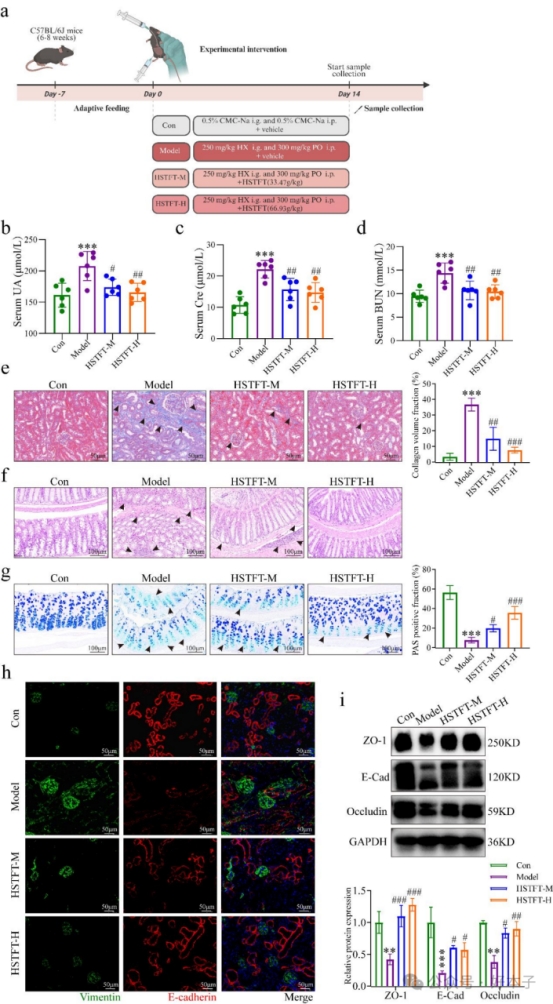
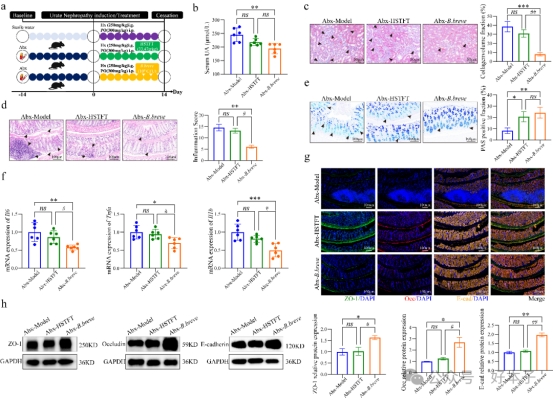
HSTFT 能减轻HUA小鼠的肾纤维化现象,并改善其肾脏功能,同时还能保护其肠道屏障。
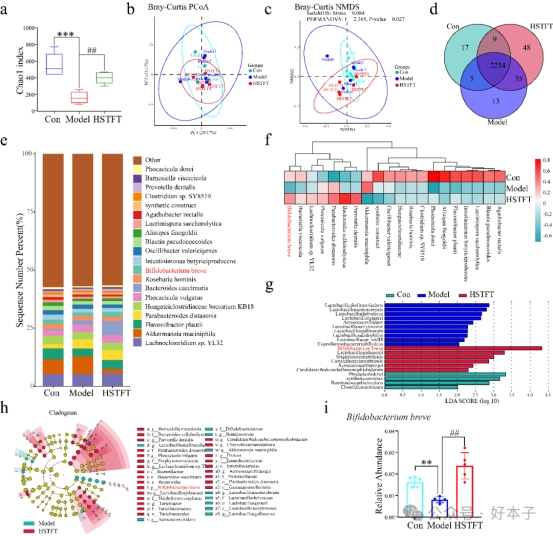
HSTFT 改变了肠道微生物群的组成,增加微生物的多样性,并提高了HUA小鼠体内有益菌(如B.breve)的含量。
HSTFT 在肠道微生物群缺失后会失去其对肾脏的保护作用,但通过B.breve的定植能够恢复其保护效果。
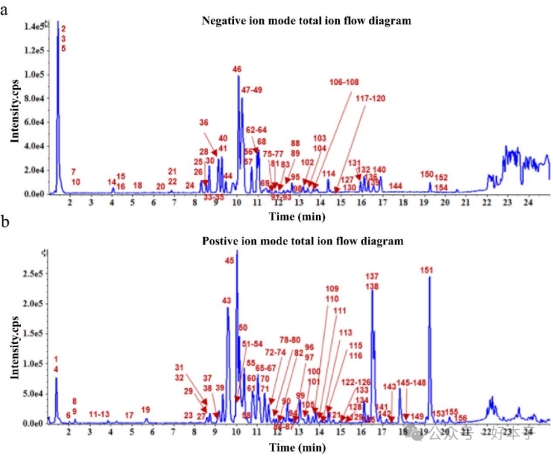
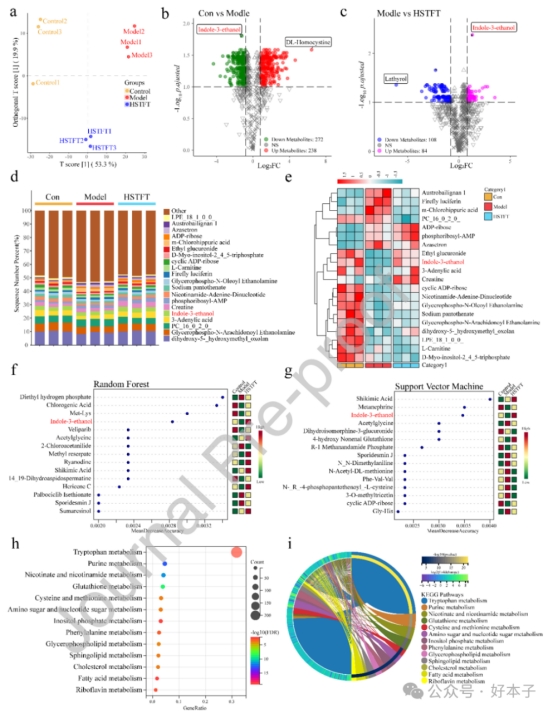
代谢组学分析鉴定出TOL为介导 HSTFT 治疗效果的关键由微生物群产生的代谢产物。
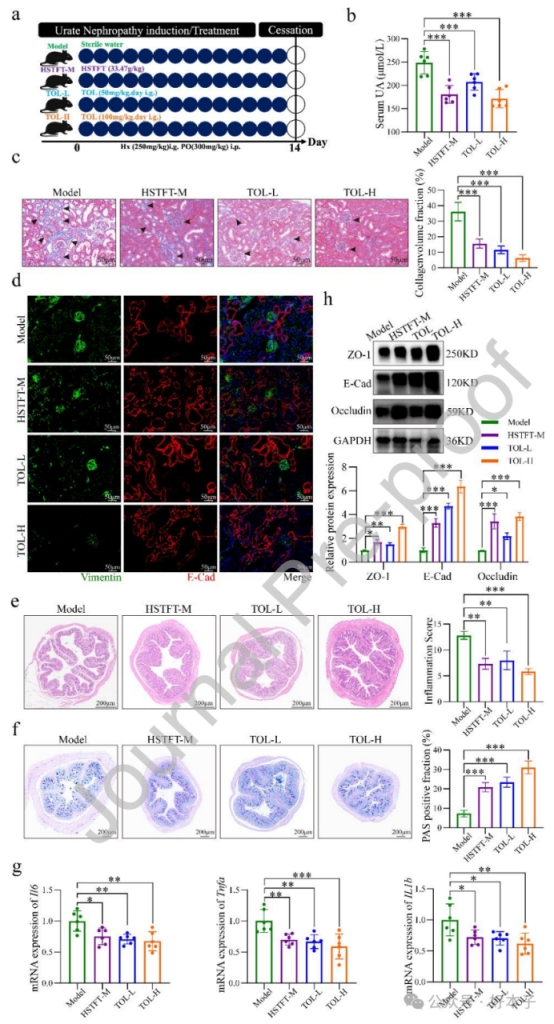
TOL能够有效地模拟 HSTFT 的治疗效果,减轻肾纤维化,保护肾小管上皮结构,并恢复肠道屏障功能。TOL能够抑制炎症并强化上皮连接,从而重建肠道与肾脏之间的平衡,并减轻HUA引起的肾脏损伤。
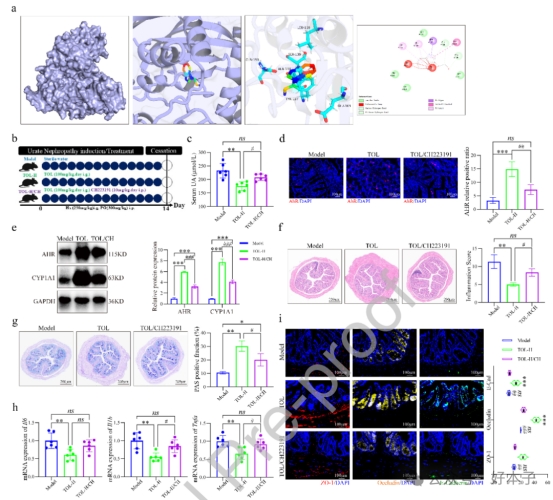
分子对接结合药理抑制实验发现,TOL通过激活AhR信号级联反应,发挥细胞保护、抗凋亡和抗炎的作用。AhR 的激活会增强上皮连接基因的转录,维持屏障的完整性,并抑制炎症细胞因子的产生,从而在有害条件下维持黏膜的稳态。抑制 AhR 的药理作用则完全消除了这些益处,证实了 AhR 是 TOL 维持肠道上皮稳定性和免疫平衡的关键分子靶点。
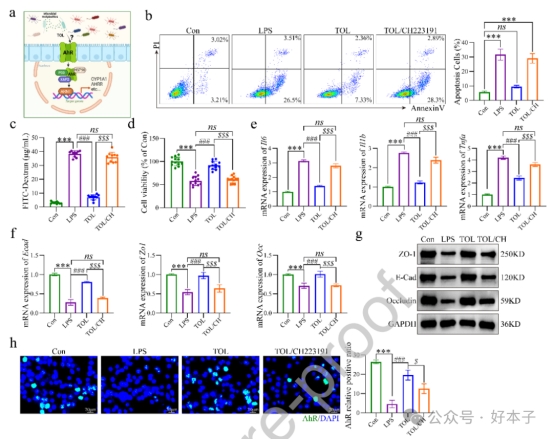
抑制AhR会消除TOL抗炎、屏障修复和肾脏保护作用,证实了微生物源性TOL-AhR轴是 HSTFT 在高尿酸血症引起的肾病中的治疗效果的基础。