冬天,来一杯热奶茶真是再适合不过了,捧在手里暖,喝进肚里甜。奶茶似乎总自带某种魔法,一口接一口,根本停不下来。如果要问奶茶的「拥趸」们为什么如此「上头」,他们八成还会给一个让人哭笑不得的解释:“日子太苦,需要奶茶来续甜。”
川大华西医院研究团队发表于Signal Transduction and Targeted Therapy(STTT)的一项最新研究[1]还是给这杯「冬日风味」泼了盆冷水。研究团队首次发现:高果糖摄入会激活mTORC1路径并增加活性氧(ROS)水平,这一「内外夹击」让Th1和Th17这些促炎型T细胞变得格外「亢奋」,从而进一步放大肠道炎症,推动结肠炎和炎症性肠病(IBD)的恶化。

首先,研究者连续两个月用「高果糖水」喂养小鼠,对照组小鼠饮用普通水。
这些尝到「甜头」的小鼠血清中果糖含量飙升,原本该保持平衡的T细胞开始「站队」。在结肠、脾脏、肠系膜淋巴结和肝脏中,Th1和Th17这些促炎型细胞比例明显增多;但负责调节和平息炎症的Tr1、Th2和Treg却几乎没变。这意味着,果糖不是无差别让免疫系统「乱作一团」,而是精准地给促炎通路踩下了「油门」,埋下之后肠道炎症的隐患。
那这股「果糖助燃」到底能把炎症推到什么程度?研究者开始上模型。他们首先在硫酸葡聚糖钠(DSS)诱导的结肠炎小鼠模型中发现,饮用普通水的对照组小鼠结肠长度基本维持在正常范围,炎症评分较低,结肠和脾脏内的Th1细胞仅处于基础激活状态,整体肠道免疫环境相对稳定。相比之下,高果糖组小鼠肠道炎症被显著放大。它们结肠明显缩短,炎症评分显著升高,同时结肠和脾脏中Th1细胞比例同步上升。换言之,高果糖进一步推高了Th1细胞介导的促炎反应,使原本已受损的肠道炎症状态持续恶化。
在此基础上,研究者进一步引入了T细胞转移模型,评估了高果糖对免疫驱动型肠炎的影响。在对照组中,小鼠虽然还是表现出一定程度的组织损伤和炎症反应,但整体仍处于可控范围内,结肠、脾脏及肠系膜淋巴结中的Th17细胞比例维持在中等水平。然而,在高果糖条件下,炎症表型明显加重。这组小鼠组织损伤程度显著高于对照组,同时Th17细胞在上述三个免疫相关组织中的比例也一致升高。
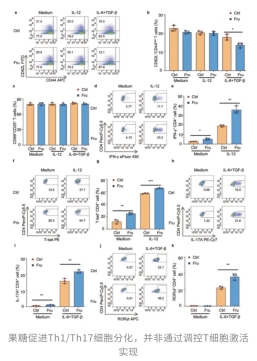
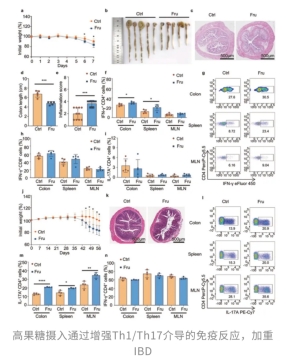
这表明高果糖专门强化了Th17细胞的生成与活化,而Th17细胞的增多会进一步分泌大量促炎细胞因子,加剧肠道免疫紊乱和组织损伤,让炎症反应在多个免疫组织中同步升级。
这就让人很困惑了,T细胞到底是怎么「感知」果糖,并做出反应的?按传统观点,促炎T细胞主要靠果糖转运蛋白GLUT5把果糖搬进细胞,用来提供能量和生物合成原料。但本研究的RNA-seq分析却给出了一记「反直觉」重击:原来,这些T细胞几乎不表达GLUT5。换言之,它们没法像利用葡萄糖那样高效「吃」果糖。
既然果糖这个「燃料」用不上,T细胞还能靠什么维持战斗力呢?
此时,便轮到「谷氨酰胺」登场了。非靶向代谢组学分析显示,果糖处理的T细胞中,谷氨酰胺水平明显升高。这种氨基酸可以转化为α-酮戊二酸,为三羧酸循环提供「燃料」,成为糖受限时的备用能量和碳源。
基于此,研究团队提出了「代谢补偿」的设想,果糖环境剥夺了T细胞高效利用糖的能力,迫使细胞启动「Plan B」,增强谷氨酰胺代谢来维持生存和功能。
有了这个线索,研究者进一步追踪下游信号通路,发现果糖通过增强谷氨酰胺代谢,激活了mTORC1信号,从而推动Th1和Th17细胞分化。当他们加入mTORC1抑制剂雷帕霉素,这种果糖带来的促炎效应就被彻底抑制了。
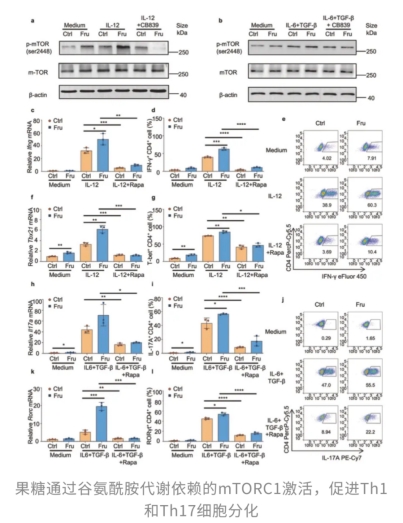
不过,高果糖还有另一条「兴风作浪」的途径,可以说「一坏,坏一窝」!研究团队早先发现,高葡萄糖能够通过产生活性氧(ROS)激活潜伏的TGF-β,从而推动Th17细胞分化。在本研究中,他们惊喜发现,果糖也能让T细胞产生ROS,水平甚至与葡萄糖相当。并且,果糖浓度越高,Th17分化越明显,呈现出明显的剂量依赖性。这说明,除了前面提到的谷氨酰胺–mTORC1轴,高果糖能通过ROS-TGF-β这条通路,特异性地为Th17细胞的分化「添柴加火」。
这也让研究者立刻想到了「二甲双胍」这款广泛用于治疗2型糖尿病的药物,因为它具有抗炎和抑制mTORC的潜力。在细胞实验中,它既能抑制果糖诱导的mTORC1磷酸化,也能减少ROS的产生。可谓双管齐下,同时阻断了两条促炎通路,从而有效逆转高果糖对Th1和Th17细胞分化的促进作用。
不过,「纸上得来终觉浅」,关键还得看在活体中的效果。研究人员又回到小鼠模型,给长期饮用高果糖水的小鼠加用二甲双胍。不出所料,二甲双胍不仅显著降低了小鼠结肠、脾脏等组织中异常升高的Th1、Th17细胞水平,更在DSS诱导的结肠炎模型中,实实在在地减轻了高果糖导致的结肠缩短和组织炎症损伤。
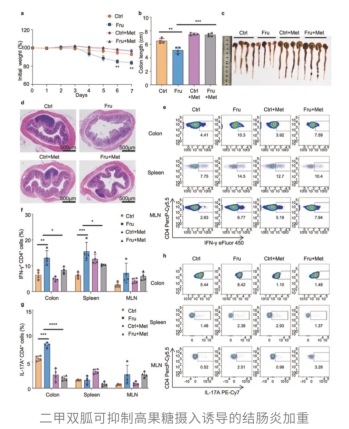
果糖让癌细胞“如虎添翼”,促结直肠癌转移当然,高果糖还有其他的「恶」没作完!
来自天津医科大学肿瘤研究所的团队发表于Gut的一项研究[2]就揭开了高果糖「作恶多端」的另一面。这项研究发现,高果糖的添加不仅能满足味蕾,还能让癌细胞如虎添翼,通过「挑拨离间」肿瘤微环境中的成纤维细胞(CAFs),助推结直肠癌的转移。

在葡萄糖供应不足的情况下,癌细胞会通过转运蛋白GLUT5大量摄取果糖,以维持自身的增殖和迁移能力。研究团队在对473例结直肠癌患者的分析中发现,GLUT5高表达的患者总体生存期明显缩短。这意味着,果糖代谢活跃与肿瘤恶化存在密切关联。与此同时,肿瘤微环境中的癌症相关成纤维细胞(CAFs)也会被果糖「唤醒」,与癌细胞形成一种「代谢盟友」关系。这时候,癌细胞将果糖代谢后的氨基酸等小分子释放出来,供CAFs利用,从而增强它们的增殖和迁移能力。这么说,CAFs也会「吃」果糖,果糖不仅「喂饱」了癌细胞,也让微环境里的CAFs变得更「能跑能打」,共同为肿瘤的生长和扩散创造了温床。而且,这些被激活的CAFs高表达趋化因子CXCL14,通过Erk信号通路反向作用于癌细胞,从而推动其侵袭和转移能力。从机制上来说,果糖不仅直接作用于癌细胞,还通过CAF-CXCL14-Erk轴间接「助推」癌细胞的侵袭与转移能力。
水果和蜂蜜中不就天然存在果糖吗?难道以后这些都要「戒」了吗?
其实,在给它们「判死刑」时,也还是不能忽视其中的「善良面」。当我们吃水果时,果糖并不会「单枪匹马」冲进体内,它被膳食纤维、维生素和抗氧化物质层层包裹。因此,对代谢系统的冲击是比较温和的。但那些藏在奶茶、汽水、蛋糕里的「游离果糖」就比较「嚣张」了,它们大多以高果糖玉米糖浆的形式存在。很容易一不小心就「炫」多了。过多的果糖就这么一路横冲直撞,进而扰乱代谢。
当然,蜂蜜作为一种天然混合物也有其「高光时刻」。除了果糖、葡萄糖和蔗糖等成分,它还富含多酚、维生素、酶和矿物质等生物活性成分。这些天然成分调节果糖吸收速度的同时,也能发挥抗氧化和抗炎作用。这样一来,或许就能缓冲一部分高果糖摄入的危害。不过,对于已经存在胰岛素抵抗、肥胖、特定肠道疾病和肿瘤的人群,对添加糖的摄入还是得慎之又慎。
[1]Ma, X., Chen, J., Wang, F.et al. High fructose consumption aggravates inflammation by promoting effector T cell generation via inducing metabolic reprogramming. Sig Transduct Target Ther 10, 271 (2025). https://doi.org/10.1038/s41392-025-02359-9
[2]Cui, Y., Liu, H., Zhang, L., et al. (2025). Fructose drives colorectal cancer progression by regulating crosstalk between cancer-associated fibroblasts and tumour cells.Gut. Advance online publication. https://doi.org/10.1136/gutjnl-2025-335014
