阿尔茨海默氏病(AD)是痴呆症的最常见形式,其特征在于与年龄相关的大脑神经变性,导致进行性认知功能减退,AD的典型组织病理学特征是淀粉样蛋白β斑块和神经原纤维缠结以及神经炎症。神经炎症是阿尔茨海默氏病(AD)疾病进展的主要因素,其特征是大脑驻留神经胶质细胞(特别是小胶质细胞)的活性。然而,越来越多的证据表明,外周血免疫细胞在AD进展和某些疾病病理的某些阶段会渗入大脑。然而,CD8 + T细胞在AD脑中的功能作用尚未完全探讨。因此,萨尔斯堡医学大学分子再生医学研究所MS Unger 团队对CD8+T细胞在AD患者脑内的作用进行了探究。
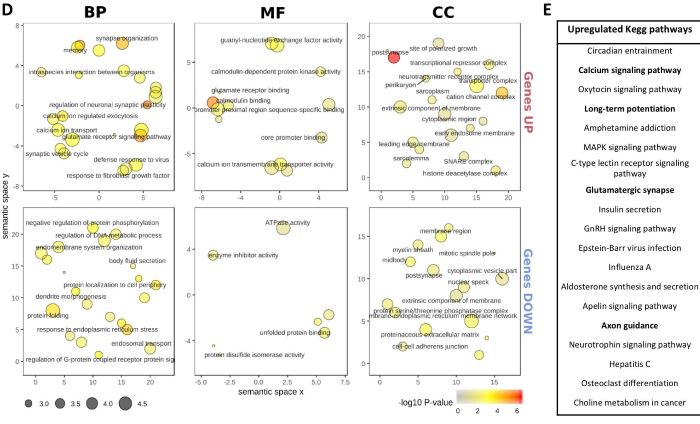
研究人员选用了APP-PS1转基因小鼠和阿尔兹海默症患者死后海马体切片探究CD8+T细胞在AD患者脑中的功能。对APP-PS1和WT小鼠进行T细胞消融实验、行为测试——莫里斯水迷宫、流式细胞术分析小鼠的静脉血及脑部组织、免疫荧光组化、qPCR进行RNA分离及基因表达分析、RNAseq分析、血液细胞因子水平分析等一系列实验后。发现APP-PS1转基因小鼠的脑实质中的CD8 + T细胞与小胶质细胞以及神经元结构紧密相关。并证明了APP-PS1小鼠和人患AD死后脑实质内海马体中的CD8 +T细胞的数量增加。此外,衰老的WT小鼠表现出CD8 + T细胞的显着浸润,这种浸润在APP-PS1小鼠中更为明显且发病较早。为了解决它们在AD中的功能相关性,研究人员使用抗CD8抗体治疗成功消融了12个月大的APP-PS1和WT小鼠的血液,脾脏和大脑中的CD8 + T细胞群,总共进行了4周。虽然在疾病现阶段的治疗既不影响认知结果也不影响斑块病理,但缺少CD8 +T细胞的APP-PS1小鼠海马体转录组的RNAseq分析显示神经元和突触相关基因的表达发生了很大变化,其中包括神经元立即早期基因(IEG)的上调,例如活动调节的细胞骨架相关蛋白(Arc)和神经元PAS域蛋白4(Npas4)。GO富集分析表明,CD8 + T细胞消融后,生物学过程“调节神经元突触可塑性”和细胞成分“突触后”被过度表达。此外,Kegg通路分析显示“钙信号传导”,“长期增强”,“谷氨酸能突触”和“轴突指导”途径上调。因此,我们得出的结论是,CD8 + T细胞会渗透到老年人和AD脑中,并且大脑CD8 + T细胞可能直接参与调节突触可塑性的神经元功能障碍。进一步的分析对于揭示CD8 + T细胞如何调节神经元景观从而促进AD病理的确切机制至关重要。(成仪型整理)